

O protozoário Leishmania infantum, causador da leishmaniose visceral, pode afetar baço, medula óssea, fígado e gânglios linfáticos (imagem: Francis W. Chandler/CDC/Wikimedia Commons)
Em menos de duas horas, exame desenvolvido na UFSCar identifica com precisão o agente causador do quadro, possibilitando um tratamento mais direcionado. Casos de coinfecção pelos protozoários Leishmania infantum e Crithidia têm crescido no país
Em menos de duas horas, exame desenvolvido na UFSCar identifica com precisão o agente causador do quadro, possibilitando um tratamento mais direcionado. Casos de coinfecção pelos protozoários Leishmania infantum e Crithidia têm crescido no país
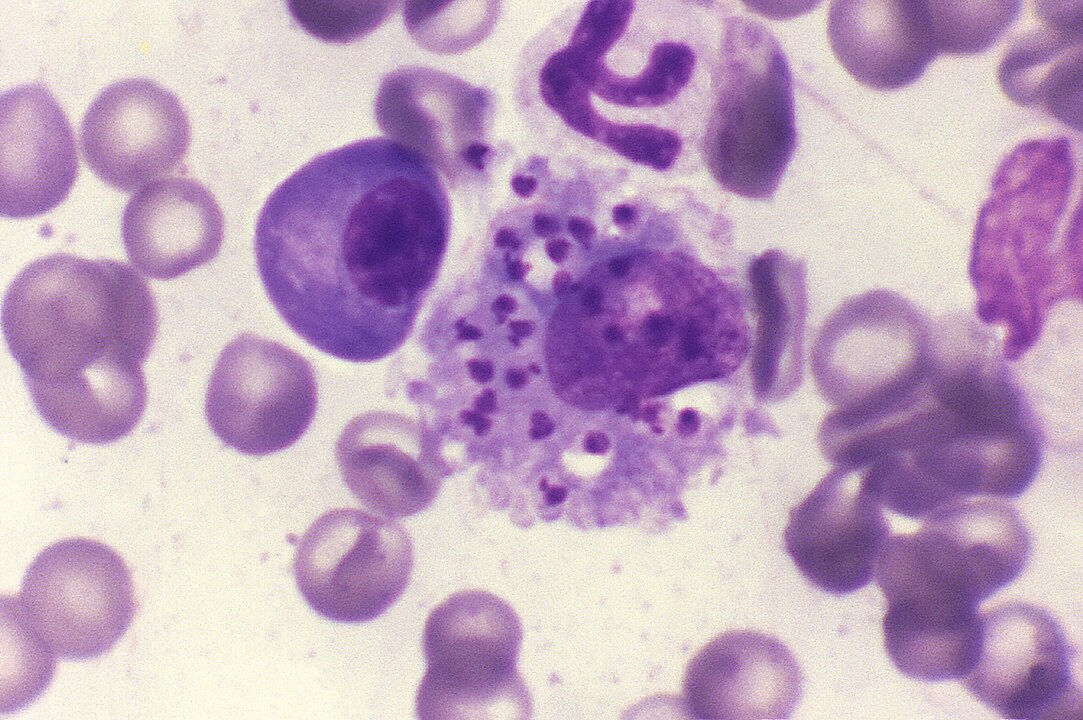
O protozoário Leishmania infantum, causador da leishmaniose visceral, pode afetar baço, medula óssea, fígado e gânglios linfáticos (imagem: Francis W. Chandler/CDC/Wikimedia Commons)
Julia Moióli | Agência FAPESP – Nos últimos anos, médicos e cientistas de regiões do Brasil onde a leishmaniose visceral (LV) é endêmica têm se deparado com cada vez mais casos de coinfecção por diferentes protozoários: Leishmania infantum e Crithidia. O diagnóstico preciso, no entanto, é dificultado pela ausência de testes simples e específicos (leia mais em: agencia.fapesp.br/42034 e agencia.fapesp.br/31573).
Com o objetivo de acelerar e facilitar essa distinção e, consequentemente, a definição do tratamento, pesquisadores da Universidade Federal de São Carlos (UFSCar) desenvolveram um teste do tipo PCR (que analisa o material genético contido na amostra) que leva menos de duas horas para ser concluído. Os resultados do estudo foram publicados no periódico Tropical Medicine and Infectious Disease.
O novo método representa um avanço no diagnóstico da LV – forma mais severa de leishmaniose que afeta órgãos como baço, medula óssea, fígado e gânglios linfáticos. Negligenciada, a doença é considerada um problema de saúde pública, com mais de 3,5 mil casos todos os anos no país, de acordo com o Ministério da Saúde. Esse número representa 93% de todos os casos da América Latina. Somente em 2020, foram 165 mortes em território nacional.
O estudo – financiado pela FAPESP por meio de nove projetos (16/18527-3, 16/20258-0, 17/16328-6, 18/26799-9, 19/19789-0, 20/14011-8, 20/15771-6, 21/10358-6 e 21/12464-8) – mostrou que o método foi altamente preciso na identificação e quantificação de L. infantum e Crithidia em amostras obtidas in vitro e in vivo ou coletadas de hospedeiros (humanos, cães, gatos e vetores), por exemplo, por meio de biópsias de pele ou aspirados de medula óssea.
“Apesar de já existirem outros métodos moleculares de identificação de espécies, eles costumam envolver o sequenciamento do DNA da amostra, processo mais trabalhoso, lento e custoso”, explica Sandra Regina Costa Maruyama, professora do Programa de Pós-Graduação em Genética Evolutiva e Biologia Molecular (PPGGEv) da UFSCar e coordenadora do estudo. “Nosso teste avalia o material genético dos parasitas diretamente dos vetores e nos tecidos de pessoas e animais [gatos e cachorros].”
Ao contrário dos testes rápidos utilizados no sistema de saúde, que não detectam diretamente o parasita e sim os anticorpos produzidos contra ele, o novo ensaio quantitativo de PCR baseado em corante (qPCR) foi projetado e padronizado com sequências-alvo específicas para as espécies Leishmania infantum e Crithidia em amostras experimentais e clínicas. Os novos alvos se mostraram específicos, entretanto é necessário realizar inicialmente um ensaio para detectar o primeiro parasita e, na sequência, um segundo para identificar Crithidia.
“Selecionamos esses novos alvos por meio de análises dos genomas das duas espécies. Agora que mostramos que apresentam especificidade em diferentes tipos de amostras, é necessário otimizar o ensaio para que em uma única reação de qPCR saibamos se a espécie infectante em questão é Leishmania infantum, Crithidia ou ambas”, diz Maruyama.
Atualmente, o grupo de pesquisa tem testado as amostras para deteção de L. infantum e, num segundo teste, faz a detecção de Crithidia. Segundo a pesquisadora, qualquer laboratório de diagnóstico capacitado com equipamento de qPCR – que se tornou mais acessível durante a pandemia de COVID-19 – poderia realizar esse teste. A técnica pode ser útil para estudos epidemiológicos, monitoramento de carga parasitária e acompanhamento terapêutico.
Casos de coinfecção
Durante o trabalho, foram realizados testes com 62 parasitas isolados dos tecidos de pacientes com leishmaniose visceral. Desses, 51 testaram positivo para Crithidia. Além disso, a coinfecção de Leishmania infantum e Crithidia em medula óssea foi identificada em dois novos casos de LV no Brasil. Em maio deste ano, o grupo publicou um relato de caso grave de LV no qual as duas espécies de parasitas foram detectadas.
De acordo com Maruyama, além da eficácia do teste, os resultados indicam que a infecção por Crithidia é mais frequente do que se imaginava e a coinfecção pelos dois protozoários parece acontecer principalmente nos casos mais graves.
“Ainda não sabemos quais as implicações clínicas da presença de Crithidia nos casos de LV, mas suspeitamos que a coinfecção possa exacerbar a doença ou até mesmo atrapalhar a resposta ao tratamento recomendado para Leishmania infantum”, diz a pesquisadora. “Identificar a espécie de parasita corretamente permite que sejam tomadas providências rapidamente para evitar a piora e a progressão do quadro clínico, reduzindo a mortalidade. Além disso, abre espaço para que, no futuro, se descubram medicamentos e tratamentos mais específicos.”
O artigo Parasite Detection in Visceral Leishmaniasis Samples by Dye-Based qPCR Using New Gene Targets of Leishmania infantum and Crithidia pode ser lido em: www.mdpi.com/2414-6366/8/8/405.
Republicar
A Agência FAPESP licencia notícias via Creative Commons (CC-BY-NC-ND) para que possam ser republicadas gratuitamente e de forma simples por outros veículos digitais ou impressos. A Agência FAPESP deve ser creditada como a fonte do conteúdo que está sendo republicado e o nome do repórter (quando houver) deve ser atribuído. O uso do botão HMTL abaixo permite o atendimento a essas normas, detalhadas na Política de Republicação Digital FAPESP.





