

Los investigadores de la USP analizaron tejidos de nueve pacientes que murieron de COVID-19 (ilustración: Elia Caldini)
En un artículo publicado en el Journal of Applied Physiology, científicos de la Universidad de São Paulo (Brasil) demuestran que el daño que el SARS-CoV-2 le causa al revestimiento de pequeños vasos pulmonares es un fenómeno determinante para el agravamiento de la enfermedad
En un artículo publicado en el Journal of Applied Physiology, científicos de la Universidad de São Paulo (Brasil) demuestran que el daño que el SARS-CoV-2 le causa al revestimiento de pequeños vasos pulmonares es un fenómeno determinante para el agravamiento de la enfermedad
Los investigadores de la USP analizaron tejidos de nueve pacientes que murieron de COVID-19 (ilustración: Elia Caldini)
Por Maria Fernanda Ziegler | Agência FAPESP – Las trombosis en los pequeños vasos (capilares) de los pulmones constituyen una de las primeras consecuencias del COVID-19 grave, que precede incluso a la dificultad respiratoria ocasionada por el denominado daño alveolar difuso. Esto fue lo que se comprobó en el marco de un estudio brasileño publicado en el Journal of Applied Physiology. Con base en las autopsias de nueve pacientes que murieron luego desarrollar la forma grave de la enfermedad, fue posible observar un cuadro muy característico, con alteraciones en la vascularización pulmonar y trombosis.
En dicho trabajo, los investigadores describen por primera vez aspectos relacionados con el daño endotelial y la formación de trombos ocasionados por la infección. Estos descubrimientos –entre ellos la constatación de que el COVID-19 tiene como carácter central la formación de trombos en la microcirculación pulmonar– aportan a la comprensión de la fisiopatología de la afección y al desarrollo de nuevas estrategias terapéuticas.
“Este estudio fue la prueba final de lo que veníamos advirtiendo desde el comienzo de la pandemia: el COVID-19 grave es una enfermedad trombótica. El virus SARS-CoV-2 posee un tropismo por el endotelio [es atraído hacia ese tejido], la capa de células que reviste los vasos sanguíneos. Por ende, al invadir las células endoteliales, afecta primeramente a la microcirculación. El problema empieza en los capilares pulmonares para luego ir coagulando los vasos mayores y afectar a cualquier otro órgano”, explica la neumóloga Elnara Negri, docente de la Facultad de Medicina de la Universidad de São Paulo (FM-USP), coautora del artículo y una de las primeras investigadoras del mundo en trabajar con esta hipótesis (lea más en: agencia.fapesp.br/33261).
En el estudio, apoyado por la FAPESP, los autores observaron mediante microscopía electrónica el efecto del virus en las células endoteliales de los pulmones de pacientes que murieron con COVID-19 grave en el Hospital de Clínicas (HC) de la FM-USP.
Con base en autopsias mínimamente invasivas, fue posible observar en todas las muestras la alta prevalencia de microangiopatía trombótica, la oclusión generalizada en la microcirculación por trombosis. Las muestras analizadas provenían de pacientes que fueron hospitalizados entre marzo y mayo de 2020. Todos esos pacientes fueron intubados, requirieron de terapia intensiva y murieron de hipoxia refractaria (insuficiencia respiratoria). Cabe destacar que ninguno de los pacientes incluidos en el estudio fue tratado con anticoagulantes, pues esa no era la directriz para el tratamiento de COVID-19 en aquel momento. Tampoco existían vacunas disponibles en ese entonces.
El endotelio descamado
Negri explica que existe una capa glucoproteica denominada glucocáliz que reviste el endotelio y que hace que la sangre pase naturalmente por las arterias, las venas y los capilares sin coagularse.
“Algunos estudios anteriores realizados por Helena Nader en la Unifesp [la Universidad Federal de São Paulo] demostraron que, para invadir las células, el virus se une fundamentalmente al receptor ACE-2 [la proteína presente en la superficie de diversas células del cuerpo, incluso en las del epitelio y las del endotélio del sistema respiratorio]. Pero antes se une al heparán sulfato [un polisacárido] asociado a la membrana de las células endoteliales, que forma precisamente el glucocáliz. Por ende, cuando el SARS-CoV-2 invade el endotelio, lo descama y destruye el glucocáliz. Esto resulta en una exposición tisular y en la coagulación intravascular que comienza en la microcirculación”, detalla Negri.
Como la acción inicial del virus se concreta en la microcirculación pulmonar, los análisis contrastados para la investigación de la presencia de trombos en vasos mayores, realizados en pacientes con COVID-19 grave en la época, nunca detectaron el problema tempranamente.
No obstante, según explica Negri, la disfunción endotelial es un fenómeno clave en el COVID-19, pues está directamente asociada a la activación de la respuesta inflamatoria característica de la enfermedad. “La invasión masiva del virus y la destrucción del endotelio promueven la ruptura de la barrera endotelial y el reclutamiento de células inmunitarias circulantes, activando vías relacionadas con la trombogénesis y con la inflamación”, dice.
En el trabajo, los investigadores observaron que el daño provocado en el endotelio tiende a preceder la aparición de dos características comunes en los casos de dificultad respiratoria: el escape significativo de la membrana alvéolo-capilar de los pulmones y la acumulación de polímeros de fibrina (una proteína asociada a la coagulación y al proceso de cicatrización) en los alvéolos pulmonares.
Un trabajo del mismo grupo de la FM-USP, encabezado por Thais Mauad, que comprendió análisis del transcriptoma (el conjunto de moléculas de ARN expresadas en un tejido), demostró que diversas vías asociadas a la coagulación, a la activación de las plaquetas y a la formación de trombos ya se encontraban activadas tempranamente en los pulmones de los pacientes con daño alveolar, precediendo así a la inflamación.
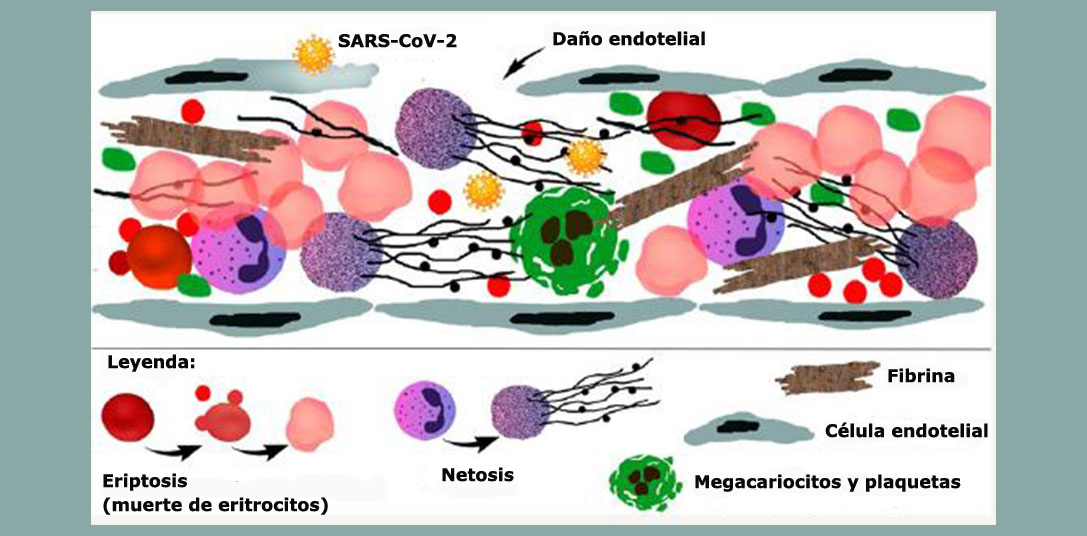
El análisis confirmó a su vez que no se trata de una coagulación común, desencadenada por la activación de los factores de coagulación. “En el COVID-19, la coagulación ocurre debido a las lesiones endoteliales y se ve potenciada por la netosis [un mecanismo inmunitario que consiste en la salida del material genético contenido en el núcleo de los neutrófilos en forma de redes –las NET– en un intento por aprisionar y matar al patógeno], por las lesiones de los hematíes con dimorfismo [una alteración morfológica de los glóbulos rojos de la sangre] y por la activación plaquetaria. Por lo tanto, existe toda una estructura para que la sangre se vuelva más densa y provoque tantas complicaciones”, afirma.
La investigadora subraya también que, ante este panorama, en donde la sangre se vuelve muy viscosa y altamente trombogénica, el paciente debe mantenerse hidratado, a diferencia de lo que se recomienda para el tratamiento del daño alveolar difuso. “Asimismo, el timing y el control riguroso de la anticoagulación son fundamentales”, advierte.
No por casualidad, otro estudio del mismo grupo, que contó con la participación de las investigadoras Marisa Dolhnikoff y Elia Caldini, demostró que el daño pulmonar en los casos graves de COVID-19 está asociado al nivel de netosis. Al analizar muestras de tejidos de autopsias pulmonares, los científicos observaron que cuanto más elevado era el nivel de NET, mayor era el daño pulmonar de los pacientes.
Negri comenta que empezó a sospechar con respecto a la relación entre el COVID-19 y la trombosis al comienzo de la pandemia, cuando detectó un cuadro muy parecido al de pacientes cardíacos que había tratado hacía más de 30 años. Tras la cirugía cardíaca, esos pacientes en aquel tiempo también exhibían microcoagulación vascular, pero eso sucedía porque se habían sometido a un tratamiento denominado circulación extracorpórea con oxigenadores de burbuja, aparatos que ya no se utilizan en medicina precisamente porque causan daño endotelial.
“Era una técnica muy utilizada hace 30 años, pero que provoca una lesión pulmonar muy parecida a la del COVID-19. En otras palabras, yo ya había visto eso. Aparte de la lesión pulmonar, otra similitud entre ambas situaciones es la existencia de fenómenos trombóticos periféricos, como el del dedo del pie morado, por ejemplo”, comenta.
“Como en el COVID-19 grave la caída inicial de la oxigenación en la sangre es secundaria a la trombosis de los capilares pulmonares y no existe inicialmente una acumulación de líquido en los pulmones, el órgano no queda ‘empapado’ ni pierde su compliancia o complacencia. Esto quiere decir que el pulmón del paciente con COVID-19 grave inicial no parece una esponja llena de líquido, tal como sucede con los pacientes con síndrome de dificultad respiratoria. Al contrario: cuando se instaura la insuficiencia respiratoria asociada al COVID-19 grave, los pulmones están deshidratados y, pese a que el aire llega hasta el alvéolo pulmonar, no logra pasar a la circulación a causa de la formación de coágulos”, explica.
Negri comenta que, en esos casos, el paciente logra llenar fácilmente sus pulmones de aire, pero el oxígeno no pasa a la sangre, pues los capilares se encuentran obstruidos. “Esto explica la llamada happy hypoxia [hipoxia feliz], es decir: el paciente no siente que su oxigenación está baja y no siente falta de aire”, dice.
Al presenciar la intubación de una paciente con COVID-19 grave, la investigadora constató que era necesaria una propuesta de tratamiento diametralmente distinta a la que se concretaba al comienzo de la pandemia.
“El secreto para tratar al paciente con COVID-19 grave es mantenerlo hidratado y aplicarle anticoagulantes en la dosis adecuada, chequeando el nivel adecuado de anticoagulación en el ambiente hospitalario tan pronto como empieza a desaturar, es decir, a experimentar una mengua de oxígeno en la sangre. Luego de ello es necesario mantener el control diario de los niveles terapéuticos de anticoagulación mediante análisis de sangre, siempre en el ambiente hospitalario para que no haya riesgo de sangrado, y la profilaxis de cuatro a seis semanas en promedio tras el alta, que es el tiempo necesario para que se reconstituya el endotelio”, comenta.
La investigadora explica que este protocolo con hidratación y el uso de anticoagulantes se produce porque, a diferencia de los otros síndromes agudos respiratorios (SARS), en los cuales el problema de la falta de paso del oxígeno desde los pulmones hacia la sangre está relacionado fundamentalmente con la inflamación en los alvéolos pulmonares, en el COVID-19 grave inicial el daño endotelial de los capilares pulmonares es predominante.
“Era precisamente esa diferencia entre el COVID-19 y los otros síndromes respiratorios agudos graves lo que no se conocía cuando la pandemia empezó. Fue por eso incluso que tantos pacientes murieron en las UTI [las unidades de terapia intensiva] de Italia, por ejemplo. El protocolo de tratamiento que se aplicaba en aquel momento era otro”, recuerdo.
En 2020 mismo, antes del trabajo publicado en el Journal of Applied Physiology, el grupo de Negri ya había observado que la aplicación de heparina (un anticoagulante) mejoró la oxigenación de los pacientes críticos. Al año siguiente, en colaboración con colegas de diversos países, los investigadores realizaron un ensayo clínico aleatorizado en el que pudieron demostrar que el tratamiento con heparina disminuyó la mortalidad en casos graves de COVID-19. Los resultados se publicaron en el British Medical Journal (lea más en: agencia.fapesp.br/37176).
“Este estudio contribuyó para modificar las directrices de tratamiento del COVID-19 en el mundo, pues pudimos demostrar la disminución de un 78 % del riesgo de mortalidad cuando se puso en marcha la anticoagulación en pacientes que necesitaban recibir oxigenación, pero aún no estaban en la UTI”, comenta la investigadora.
Negri destaca que es perentorio revertir la disfunción endotelial en los casos de COVID-19 grave mediante el uso de anticoagulantes. “Es necesario tratar la coagulación cuanto antes, pues esto es crucial para evitar el desarrollo del síndrome respiratorio agudo y otras derivaciones de la enfermedad, tal como es el caso del llamado COVID largo”, dice.
Otro estudio recientemente publicado en Nature Medicine por científicos británicos refuerza el carácter de la formación de trombos del SARS-CoV-2. En dicho trabajo, los únicos marcadores de pronóstico para el COVID largo identificados fueron el fibrinógeno y el dímero D, dos proteínas asociadas a la coagulación.
“Este estudio muestra que el COVID largo es producto de la trombosis no tratada adecuadamente. El problema en la microcirculación puede persistir en diversos órganos, incluso en el cerebro, en el corazón y en los músculos, como si el paciente sufriese pequeños infartos”, explica Negri.
Puede leerse el artículo intitulado Ultrastructural characterization of alveolar microvascular damage in severe COVID-19 respiratory failure en el siguiente enlace: journals.physiology.org/doi/abs/10.1152/japplphysiol.00424.2023.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





