

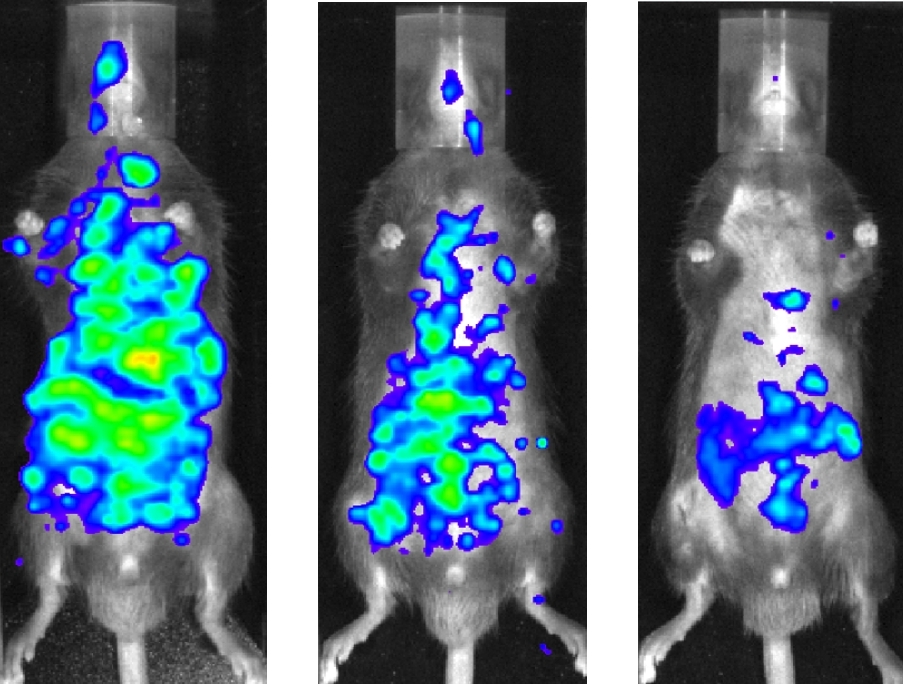
El grado de inflamación en los ratones se midió mediante el empleo del IVIS (In vivo imaging system) (imagen: divulgación)
La destrucción de los hematíes, común en pacientes con anemia falciforme, provoca una inflamación sistémica y perjudica la circulación sanguínea
La destrucción de los hematíes, común en pacientes con anemia falciforme, provoca una inflamación sistémica y perjudica la circulación sanguínea
El grado de inflamación en los ratones se midió mediante el empleo del IVIS (In vivo imaging system) (imagen: divulgación)
Por Karina Toledo
Agência FAPESP – En pacientes con anemia falciforme, es común que ocurra un fenómeno conocido como hemólisis, caracterizado por la destrucción de los glóbulos rojos de la sangre o hematíes, y la consiguiente liberación en el torrente sanguíneo de la proteína hemoglobina existente en su interior.
Estudios recientes han mostrado que este fenómeno contribuye fuertemente al agravamiento de la enfermedad. Cuando sucede de manera repetida, puede llevar a un estado inflamatorio crónico y favorecer procesos vasooclusivos, que además de intensas crisis de dolor pueden causar infartos en cualquier parte del cuerpo y lesionar diversos órganos.
En un artículo destacado en el editorial de la edición del día 6 de agosto de la revista Blood, investigadores de la Universidad de Campinas (Unicamp), en São Paulo, Brasil, mostraron que algunas de las complicaciones derivadas de la hemólisis pueden prevenirse con una droga llamada hidroxiurea, ya utilizada en el tratamiento crónico de la anemia falciforme, pero con un propósito distinto.
“Creemos que la hidroxiurea está siendo subutilizada. Pretendemos hacer un ensayo clínico para evaluar la eficacia de este fármaco en el combate contra la inflamación aguda inducida por la hemólisis y en el tratamiento de crises vasooclusivas”, afirmó Nicola Conran, investigadora del Centro de Hematología y Hemoterapia (Hemocentro) de la Unicamp y coautora del artículo.
La investigación se llevó a cabo con el apoyo de la FAPESP durante el posdoctorado de Camila Bononi de Almeida, supervisado por Conran, en el ámbito de un Proyecto Temático coordinado por el profesor de la Unicamp Fernando Ferreira Costa.
Según explicó Conran, la anemia falciforme es una enfermedad hereditaria caracterizada por una alteración genética en la hemoglobina, la proteína que le da la coloración rojiza a la sangre y es responsable del transporte del oxígeno a través del sistema circulatorio.
Esta mutación hace que la hemoglobina se polimerice después de que se libera el oxígeno y, por consiguiente, los hematíes asuman la forma de hoz. Las células deformadas se vuelven rígidas y propensas a adherirse al endotelio, dificultando la circulación de la sangre.
La hidroxiurea ha sido usada en el tratamiento crónico de la enfermedad con el objetivo de aumentar la producción de otra proteína conocida como hemoglobina fetal (normalmente producida en el período de vida uterina), capaz de disminuir la polimerización de la hemoglobina genéticamente alterada y reducir el riesgo de vasooclusión.
En trabajos anteriores, el grupo del Hemocentro ya había demostrado en ratones con anemia falciforme que la hidroxiurea, en dosis más elevadas, era eficaz también en el tratamiento agudo de crises vasooclusivas (lea más en portugués, en agencia.fapesp.br/16356), pues activa una vía de señalización celular dependiente de óxido nítrico que facilita la vasodilatación y dificulta la interacción entre los glóbulos blancos y rojos, y, por consiguiente, su adherencia al endotelio.
En este nuevo trabajo, mediante experimentos con ratones sanos, el grupo demostró que ese efecto “donante de óxido nítrico” de la hidroxiurea puede ser benéfico también para combatir la inflamación causada por la hemólisis.
“Cuando se libera la hemoglobina en la circulación, ésta consume el óxido nítrico existente en el interior de los vasos y eso causa vasoconstricción, dificultando el flujo sanguíneo. Nuestros experimentos demostraron que ese proceso denominado hiperhemólisis también desemboca en un proceso inflamatorio sistémico casi que inmediato, probablemente debido al consumo del óxido nítrico”, comentó Conran.
El experimento
Para inducir la hemólisis en animales sanos, los investigadores inyectaron agua por vía intravenosa. La ruptura de los hematíes provocó en tan sólo 15 minutos aproximadamente un estado inflamatorio sistémico comparable al observado en el grupo de animales que no recibieron el estímulo hemolítico del agua, pero a los cuales les aplicaron inyecciones de TNFα, una citocina reconocida en la literatura científica debido a su gran potencial de causar inflamación.
El grado de inflamación se midió mediante de una tecnología conocida como IVIS (In vivo imaging system, el sistema de imágenes en vivo), merced a una colaboración con el equipo del Centro de Terapia Celular (CTC), uno de los CEPIDs apoyados por la FAPESP, con sede en la Facultad de Medicina de Ribeirão Preto, de la Universidad de São Paulo (FMRP-USP).
Este método consiste en inyectar en los animales una molécula (sonda) capaz de reconocer y de enlazarse a sustancias producidas por células de defensa activadas. Cuando se concreta este enlace, se emite luminescencia, que puede cuantificársela. Cuanto mayor sea la cantidad de leucocitos y neutrófilos activados, mayor es la emisión de luz.
“Para estar seguros de que estaba ocurriendo la hemólisis, dosificamos el nivel de hemoglobina en el plasma sanguíneo de los roedores y vimos que éste aumentaba tras la inyección de agua, quedando equivalente al observado en animales portadores de anemia falciforme”, comentó Bononi de Almeida.
En tanto, la inflamación vascular, cuantificada por la adherencia al endotelio de los glóbulos blancos de la sangre, se evalúo mediante una técnica de microscopia intravital. “Observamos la circulación en un tejido translúcido que envuelve el saco escrotal del ratón. Esto permite ver la migración de células hacia el local inflamado y su adherencia a la pared del vaso”, dijo Almeida.
A otro grupo de ratones, los investigadores les administraron la hidroxiurea, al mismo tiempo que les inyectaron agua en el torrente sanguíneo. Se repitieron las pruebas y los resultados indicaron que, aunque se producía la destrucción de los hematíes y la liberación de la hemoglobina en la sangre, el proceso inflamatorio fue significativamente inhibido, como así también la consiguiente adherencia de células a la pared vascular.
Una gama de posibilidades
De acuerdo con Conran, aparte de los defectos genéticos en la hemoglobina, tal como es el caso de la anemia falciforme, otros factores pueden causar la destrucción de los hematíes, entre ellos determinadas drogas, traumas físicos, transfusiones con tipos sanguíneos incompatibles y enfermedades tales como la malaria, la talasemia, la sepsis y otras.
“Es posible que, en varias de esas condiciones, el uso de hidroxiurea pueda ayudar a combatir las complicaciones derivadas de la hemólisis. Pero esto es algo que aún debe ser mejor explorado. Este trabajo abre un gran abanico para la realización de nuevas investigaciones”, concluyó Conran.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





