

En pruebas realizadas en ratones y en cultivos in vitro, una molécula diseñada en el Centro de Investigación e Innovación en Biodiversidad y Fármacos de la FAPESP fue capaz de matar al parásito del paludismo (imagen: CIBFar)
En pruebas realizadas en ratones y en cultivos in vitro, una molécula diseñada en el Centro de Investigación e Innovación en Biodiversidad y Fármacos de la FAPESP fue capaz de matar al parásito del paludismo
En pruebas realizadas en ratones y en cultivos in vitro, una molécula diseñada en el Centro de Investigación e Innovación en Biodiversidad y Fármacos de la FAPESP fue capaz de matar al parásito del paludismo
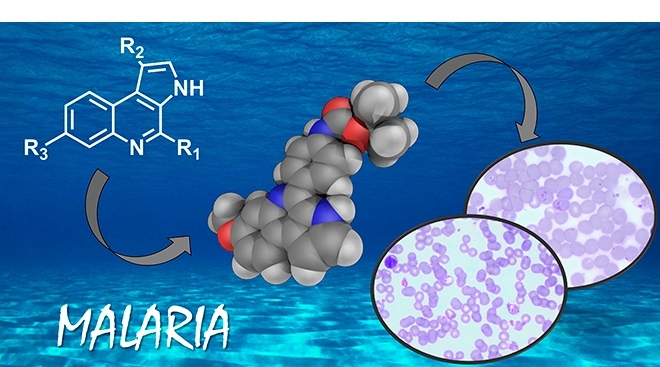
En pruebas realizadas en ratones y en cultivos in vitro, una molécula diseñada en el Centro de Investigación e Innovación en Biodiversidad y Fármacos de la FAPESP fue capaz de matar al parásito del paludismo (imagen: CIBFar)
Por Maria Fernanda Ziegler | Agência FAPESP – Una nueva molécula sintetizada en laboratorio surge como una fuerte candidata para el desarrollo de un fármaco contra la malaria. La posibilidad de que haya un nuevo medicamento contra esta enfermedad aporta esperanza a miles de pacientes infectados por el Plasmodium falciparum, uno de los protozoos causantes del paludismo, fundamentalmente porque las pruebas mostraron que la molécula mencionada fue capaz de matar incluso a la cepa resistente a los antipalúdicos convencionales.
Esta molécula exhibe baja toxicidad y un alto poder de selectividad, al actuar únicamente sobre el protozoario y no sobre otras células del organismo del huésped. La misma deriva del tipo de las marinoquinoleínas, con destacada actividad biológica, y se la desarrolló en Brasil, en el Centro de Investigación e Innovación en Biodiversidad y Fármacos (CIBFar), un Centro de Investigación, Innovación y Difusión (CEPID) financiado por la FAPESP. El estudio contó también con el apoyo económico del Consejo Nacional de Desarrollo Científico y Tecnológico (CNPq) de Brasil y del Instituto Serrapilheira.
En un artículo publicado en Journal of Medicinal Chemistry, los científicos describen la acción inhibitoria de la molécula en la fase sanguínea y hepática del ciclo asexuado del protozoario, responsable de los signos y síntomas de la enfermedad.
Aparte de los estudios realizados con cepas de cultivo in vitro, los investigadores también testearon la molécula en ratones. “En las pruebas realizadas al quinto día de estudio, la molécula logró disminuir en un 62% de la cantidad de parásitos presentes en la sangre (parasitemia). Al cabo de los 30 días de pruebas, todos los ratones que ingirieron doses de la molécula sobrevivieron”, declaró Rafael Guido, docente del Instituto de Física de São Carlos (IFSC) de la Universidad de São Paulo (USP) y uno de los autores del artículo, a Agência FAPESP.
Las pruebas se concretaron en un modelo animal infectado por P. berghei, dado que el P. falciparum no infecta a los ratones.
La inspiración llegó proveniente del mar
La molécula candidata a convertirse en fármaco se sintetizó con base en compuestos naturales hallados en bacterias marinas conocidos como marinoquinoleínas, a los cuales se los evalúo al descubrírselos contra el paludismo, la enfermedad de Chagas y la tuberculosis. Sin embargo, los productos naturales presentaron tan sólo una acción entre moderada y débil contra los patógenos.
“El núcleo de esas moléculas, conocido por pirroloquinolina [que contienen el núcleo 3H-pirrolo[2,3-c]quinolínico], nos llamó la atención. Es una estructura rara entre los productos naturales y ha sido poco abordada en la literatura científica”, dijo Carlos Roque Duarte Correia, docente del Instituto de Química de la Universidad de Campinas (Unicamp).
En 2012, el grupo de investigadores de la Unicamp publicó una de las primeras síntesis de las marinoquinoleínas naturales en la literatura.
“Durante el trabajo de síntesis nos dimos cuenta del enorme potencial farmacológico de esas moléculas. Entonces efectuamos nuevas modificaciones estructurales en la parte de pirroloquinolina, empleando eficientes procesos catalíticos, y a partir de la estructura obtenida creamos una nueva molécula con una potencia ampliada centenas de veces contra el P. falciparum, y sin aumentar su toxicidad”, dijo Guido.
Duarte Correia comenta que en el estudio se testearon las 50 primeras moléculas desarrolladas a partir de las marinoquinoleínas. “Pero este trabajo no culmina con esa publicación. Aún hay una serie de compuestos en desarrollo”, sostuvo.
El grupo está caracterizando todavía el potencial de este tipo de moléculas para tratar la malaria causada por Plasmodium vivax, la forma de paludismo más prevalente en Brasil, y está desarrollando la parte de farmacocinética del proyecto, que se refiere a la reacción del organismo al medicamento.
“Si las propiedades del compuesto, tales como solubilidad, absorción, distribución, metabolismo y excreción no fueran adecuadas, éste podría acumularse en el organismo y así volverse tóxico para el paciente, lo que inviabilizaría el medicamento. Una vez que concluyamos esta etapa, nuestro objetivo consistirá en realizar las pruebas preclínicas y los ensayos clínicos”, dijo Guido.
Muerto de hambre
Los mecanismos de acción de la molécula aún no se conocen por completo. Pero se sabe que entre ellos se encuentra una vía clásica de inhibición del parásito conocida como metabolismo de hemozoína.
Esta estrategia consiste en mantener baja la concentración de este compuesto, que es tóxico para el parásito. Cuando éste se instala en el huésped, infecta en primer lugar a los hematíes (los glóbulos rojos), pues la hemoglobina presente en esas células constituye la única fuente de energía que el parásito encuentra para consumir. Pero la hemoglobina contiene una molécula de cofactor unida a su estructura llamada grupo hemo, la cual en su forma libre –cuando está desconectada de la hemoglobina– es altamente tóxica para los parásitos.
Años de evolución dotaron al parásito de la capacidad para desarrollar un mecanismo que polimeriza ese grupo para librarse así de su toxicidad. “Esta estrategia del parásito consistente en obtener energía sin intoxicarse funciona más o menos como barrer el polvo debajo de la alfombra. El grupo hemo sigue estando presente, pero en un forma polimerizada e insoluble que no es tóxica para el parásito”, dijo Guido.
La molécula que desarrolló el grupo de investigadores del CIBFar actúa –entre otros mecanismos– impidiendo esa polimerización. De este modo, el parásito es intoxicado por el grupo hemo.
“La molécula actúa impidiendo la formación del polímero hemozoína, que es la forma que el parásito desarrolló para librarse de la toxicidad del grupo hemo. Al impedir la formación de la hemozoína, el parásito se muere”, dijo Célia Regina Garcia, docente de la Facultad de Ciencias Farmacéuticas de la Universidad de São Paulo y también autora del artículo. Garcia trabajó en colaboración con el CIBFar y estuvo a cargo de las pruebas del mecanismo de acción de la molécula en el parásito.
Cepas resistentes
Otro indicador de que la molécula derivada de la marinoquinoleína es una fuerte candidata a fármaco reside en el hecho de que logra matar a las cepas resistentes a tres de los principales medicamentos contra la malaria: la cloroquina, la pirimetamina y la sulfadoxina.
“La cloroquina ha sido poco usada para el tratamiento de la malaria falciparum, que es la afección responsable de los casos más graves y fatales de la enfermedad, y se espera que la artemisinina siga el mismo camino. Actualmente la artemisinina es el principal fármaco en uso para el tratamiento del paludismo. Si bien aún es eficaz, es un fármaco con los años contados a causa de la resistencia, y esas cepas resistentes están propagándose por toda Asia. Por ende, existe una preocupación mundial en lo que hace al desarrollo de fármacos contra la malaria, y yo pienso que Brasil es un país que tiene potencial como para destacarse en esa área”, dijo Garcia.
De acuerdo con datos de la Organización Mundial de la Salud (OMS) la malaria mata actualmente a 445 mil personas por año. “Si hoy en día, con un medicamento eficaz, tenemos una cantidad tan elevada de muertes, de no desarrollarse nuevos fármacos en el futuro, el paludismo podrá matar a más gente. Es la parasitosis que más mata en el mundo, aun cuando actualmente se cuenta con un tratamiento relativamente eficaz”, dijo Guido.
Puede leerse el artículo intitulado Discovery of Marinoquinolines as Potent and Fast-Acting Plasmodium falciparum Inhibitors with in Vivo Activity (doi: 10.1021/acs.jmedchem.8b00143), de Anna Caroline Campos Aguiar, Michele Panciera, Eric Francisco Simão dos Santos, Maneesh Kumar Singh, Mariana Lopes Garcia, Guilherme Eduardo de Souza, Myna Nakabashi, José Luiz Costa, Célia R. S. Garcia, Glaucius Oliva, Carlos Roque Duarte Correia y Rafael Victorio Carvalho Guido, en el periódico científico Journal of Medicinal Chemistry, en el siguiente enlace: pubs.acs.org/doi/10.1021/acs.jmedchem.8b00143.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





