

Un trabajo del Centro de Investigación en Procesos Redox en Biomedicina (Redoxoma), en Brasil, apunta que una proteína capaz de librar a las células de un oxidante puede ubicarse en distintas partes de las mitocondrias (Arte sobre imagen: Wikimedia Commons/ Jornal da USP)
Un trabajo del Centro de Investigación en Procesos Redox en Biomedicina (Redoxoma), en Brasil, apunta que una proteína capaz de librar a las células de un oxidante puede ubicarse en distintas partes de las mitocondrias
Un trabajo del Centro de Investigación en Procesos Redox en Biomedicina (Redoxoma), en Brasil, apunta que una proteína capaz de librar a las células de un oxidante puede ubicarse en distintas partes de las mitocondrias
Un trabajo del Centro de Investigación en Procesos Redox en Biomedicina (Redoxoma), en Brasil, apunta que una proteína capaz de librar a las células de un oxidante puede ubicarse en distintas partes de las mitocondrias (Arte sobre imagen: Wikimedia Commons/ Jornal da USP)
Por Karina Toledo | Agência FAPESP – La respiración celular es un proceso que transcurre dentro de ciertos orgánulos conocidos con el nombre de mitocondrias, que suministran la energía necesaria para el funcionamiento de los organismos. Eventualmente, puede generar subproductos que son tóxicos para las células, que son las llamadas especies reactivas de oxígeno (ROS, por sus siglas en inglés).
Cuando existen en exceso, estas sustancias oxidantes interactúan con las proteínas, los lípidos, los hidratos de carbono y los ácidos nucleicos, y hacen que estas macromoléculas pierdan su función. Este proceso puede derivar en la muerte celular y, en los seres más complejos como los humanos, puede contribuir en la inducción de enfermedades tales como el cáncer, la artritis, la aterosclerosis, el párkinson y el alzhéimer.
Sin embargo, en estudios más recientes se ha demostrado que en cantidades adecuadas, las moléculas reactivas, tal como es el caso del peróxido de hidrógeno, pueden actuar como agentes señalizadores en importantes procesos celulares, y contribuir así al buen funcionamiento del organismo. A las enzimas antioxidantes les compete la misión de mantener a las especies reactivas en niveles aceptables, a los efectos de proteger a las células contra el daño oxidativo.
“La peroxirredoxina es la principal enzima encargada de remover el peróxido de hidrógeno de dentro de las mitocondrias. Por ende, ya se sabía que estaba presente en esos orgánulos, pero no se conocía el sitio exacto de su ubicación. Nuestro grupo demostró que esta proteína puede hallarse en dos subcompartimentos mitocondriales, y esto nos suministra pistas acerca de los papeles que ejerce en esos orgánulos”, comentó Luis Eduardo Soares Netto, docente del Instituto de Biociencias de la Universidad de São Paulo (IB-USP), en Brasil.
Esta investigación tuvo lugar durante el doctorado de Fernando Gomes, bajo la supervisión de Soares Netto, y contó con la colaboración de Mario Barros, docente del Instituto de Ciencias Biomédicas (ICB-USP) y experto en biogénesis mitocondrial. Este grupo está vinculado al Centro de Investigación en Procesos Redox en Biomedicina (Redoxoma), un Centro de Investigación, Innovación y Difusión (CEPID) de la FAPESP.
Aparte de mapear la ubicación de las peroxirredoxinas en las mitocondrias, los científicos también identificaron a las proteínas encargadas de realizar el transporte de esas enzimas desde el citoplasma celular, donde se las elabora, hasta los subcompartimientos mitocondriales, en donde deben actuar. Como modelo, el grupo empleó células de la especie Saccharomyces cerevisiae, la levadura del pan y de la cerveza.
Los resultados de este estudio salieron publicados en Journal of Biological Chemistry – JBC.
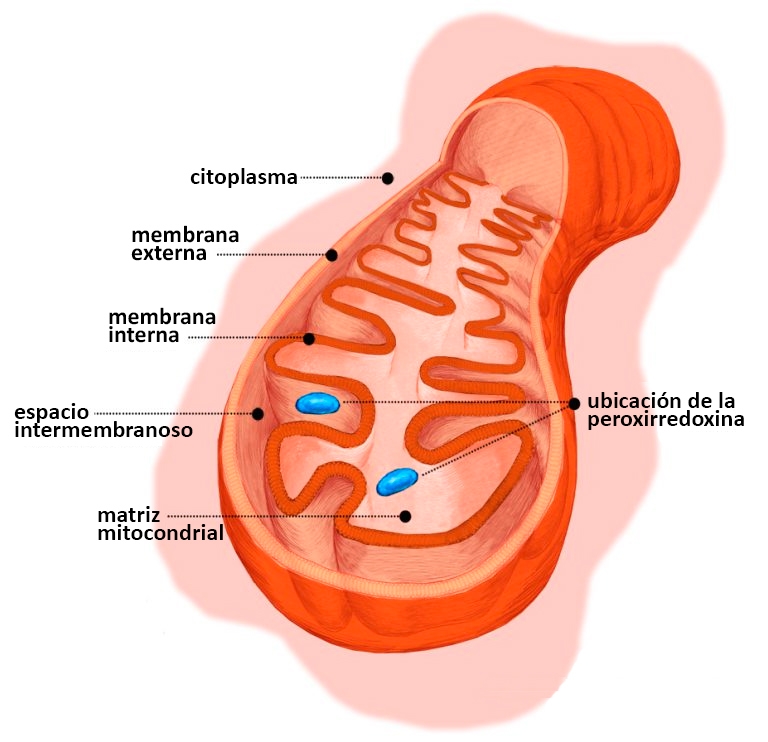
“Las mitocondrias poseen cuatro subcompartimentos: la matriz, que es la parte mayor y central, en donde se encuentra el ADN mitocondrial y en donde transcurre el ciclo de Krebs [una importante etapa de la respiración celular aeróbica], la membrana interna, en donde se produce el ATP [el trifosfato de adenosina, una molécula que almacena energía], la membrana externa, que separa a la mitocondria del resto de la célula, y el espacio intermembranoso”, explicó Soares Netto.
Según el investigador, cada subcompartimento suele contar con un conjunto específico de proteínas. La peroxirredoxina es uno de los pocos casos en que la misma proteína puede hallarse al mismo tiempo en más de un lugar dentro del orgánulo: en la matriz mitocondrial y en el espacio intermembranoso.
“Una hipótesis plausible indica que en la matriz cumple la función de proteger al ADN mitocondrial contra el daño oxidativo, en el marco de una visión más clásica del rol de las enzimas antioxidantes. En tanto, en el espacio intermembranoso, es posible que desempeñe una función regulatoria y participe en el proceso de formación de enlaces disulfuro entre las proteínas”, dijo Soares Netto.
Este tipo de unión química, que ocurre entre dos aminoácidos tipo cisteína, dota de una mayor estabilidad a las proteínas y, en algunos casos, puede resultar esencial para que la molécula ejerza sus funciones adecuadamente.
“Para que se concrete la formación del enlace disulfuro, la proteína blanco debe ser oxidada y la peroxirredoxina podría regular este proceso de transferencia de electrones dentro del espacio intermembranoso. Pero esto es algo que aún debe investigarse mejor”, dijo Soares Netto.
Uno de los proyectos futuros del grupo, según comentó el investigador, consiste en desarrollar una levadura modificada que exprese únicamente la isoforma de la peroxirredoxina presente en la matriz o sólo la isoforma encontrada en el espacio intermembranoso. “De este modo, podríamos analizar individualmente cada una de las funciones de esta enzima dentro de la mitocondria.”
Un mecanismo conservado
Al estudiar este orgánulo en levaduras, el equipo del Redoxoma observó que la peroxirredoxina es transportada inicialmente desde el citoplasma celular hacia el interior mitocondrial por una proteína llamada TOM. Cuando llega a la membrana interna, la proteína TIM23 asume la función de llevarla hasta la matriz mitocondrial. En este subcompartimento, la enzima es procesada por dos proteasas (enzimas que rompen las uniones peptídicas de otras proteínas) conocidas como MPP y Oct1, que cortan fragmentos de la molécula y hacen que ésta permanezca en ese sitio.
Sin embargo, en algunos casos, antes de que la TIM23 logre llevar a la peroxirredoxina hasta la matriz, otras dos proteasas presentes en la membrana interna –Imp1 y Imp2– procesan la enzima y hacen que permanezca a mitad de camino, para luego quedar liberada en el espacio intermembranoso.
“Son dos eventos que ocurren de manera alternativa. Sabemos que el momento en que se determina si la peroxirredoxina va a parar a la matriz o se queda en el espacio intermembranoso es cuando interactúa con la TIM23. Pero todavía no sabemos a ciencia cierta en qué contexto sucede esto”, dijo Soares Netto.
En uno de los experimentos, el grupo del IB-USP modificó genéticamente la levadura, a los efectos de hacerla expresar la peroxirredoxina humana. De este modo, fue posible verificar que la enzima es reconocida por las mismas proteínas transportadoras, y todo el proceso transcurre de manera similar al que se observa en la levadura “silvestre” (no modificada).
“El hecho de que el transporte de la peroxirredoxina hacia las mitocondrias constituya un proceso que se ha conservado en el transcurso de la evolución sugiere que éste es un evento importante, crucial para el funcionamiento de estos orgánulos”, sostuvo Soares Netto.
Y como cualquier evento que afecte a la función mitocondrial puede comprometer la supervivencia de las células, según ponderó el investigador, es posible que la peroxirredoxina o algunas de las moléculas que se encargan de su transporte hacia el interior de las mitocondrias puedan erigirse en blancos con la mira puesta en el tratamiento de enfermedades neurodegenerativas, el cáncer, la diabetes y muchas otras afecciones.
Puede leerse el artículo intitulado Proteolytic cleavage by the IMP complex or Oct1 peptidase controls the localization of the y east peroxiredoxin Prx1 to distinct mitochondrial compartments (doi: 10.1074/jbc.M117.788588) en el siguiente enlace: jbc.org/content/early/2017/08/18/jbc.M117.788588.short.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





