

Neuroesfera obtenida de células madre neurales de ratones e infectada con el virus SARS-CoV-2 adaptado. Mediante el empleo de la técnica de inmunofluorescencia, es posible observar en azul el núcleo de la célula y, en rojo, la proteína spike del coronavirus (imagen: Bruna A. G. de Melo/Unifesp)
Una biotinta desarrollada con base en células de ratones puede emplearse en impresoras 3D para generar un diseño más parecido al cerebro que los convencionales. Científicos de la Universidad Federal de São Paulo, en Brasil, obtuvieron también una versión adaptada del SARS-CoV-2 capaz de infectar a las células nerviosas de los roedores
Una biotinta desarrollada con base en células de ratones puede emplearse en impresoras 3D para generar un diseño más parecido al cerebro que los convencionales. Científicos de la Universidad Federal de São Paulo, en Brasil, obtuvieron también una versión adaptada del SARS-CoV-2 capaz de infectar a las células nerviosas de los roedores
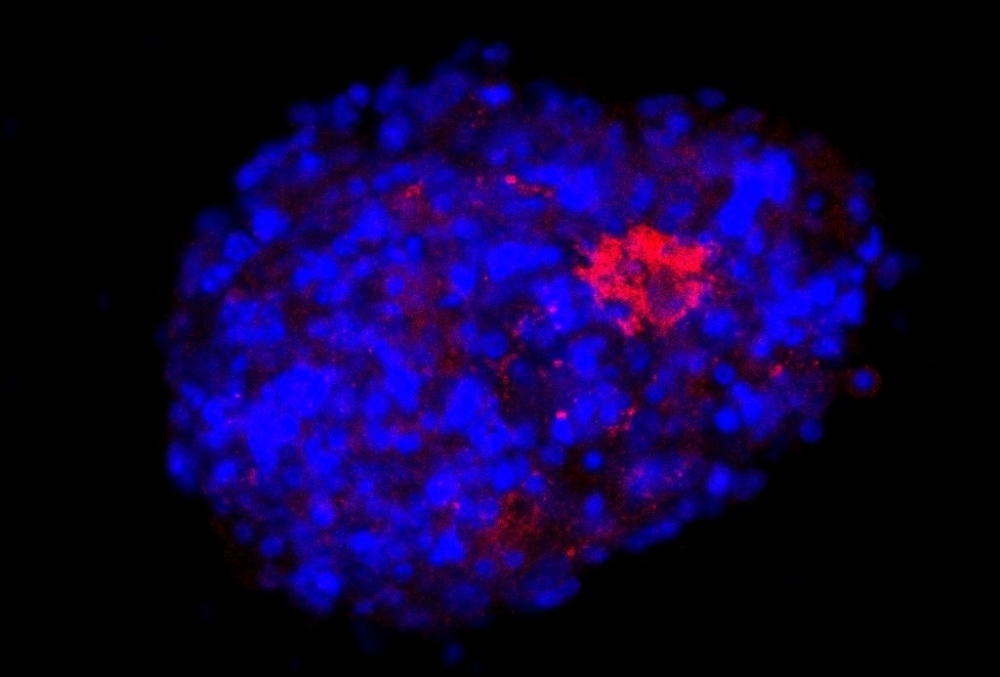
Neuroesfera obtenida de células madre neurales de ratones e infectada con el virus SARS-CoV-2 adaptado. Mediante el empleo de la técnica de inmunofluorescencia, es posible observar en azul el núcleo de la célula y, en rojo, la proteína spike del coronavirus (imagen: Bruna A. G. de Melo/Unifesp)
Por André Julião | Agência FAPESP – Científicos vinculados a la Universidad Federal de São Paulo (Unifesp), en Brasil, desarrollaron –con células de ratón– un modelo bioimpreso tridimensional del cerebro para estudiar la acción neurológica del virus SARS-CoV-2. Asimismo, los investigadores lograron crear una versión adaptada del patógeno capaz de infectar a las células nerviosas de los roedores. Y esperan que estos dos logros –descritos en la revista Advanced Biology– ayuden a abaratar y agilizar los estudios referentes a los efectos del COVID-19 sobre el sistema nervioso central.
“Nuestra propuesta consiste en crear modelos bioimpresos tridimensionales que podrían emplearse para estudiar los mecanismos de invasión del virus, la acción de fármacos y otros temas. Como el SARS-CoV-2 que infecta a los humanos no infecta a los ratones, la opción hasta ahora consistía en utilizar animales genéticamente modificados que expresan el receptor humano [la proteína ACE-2, a la cual el virus se une para invadir las células]. Pero nosotros pretendíamos arribar a una versión adaptada del virus específica para las células neurales de esos animales”, comenta Marimélia Porcionatto, docente de la Escuela Paulista de Medicina (EPM-Unifesp) y coordinadora del proyecto, que es financiado por la FAPESP.
Este trabajo contó con la colaboración de un equipo de virólogos, entre ellos Juliana Maricato y Luiz Mario Janini, docente de la EPM-Unifesp, este último también apoyado por la FAPESP.
La llamada biotinta que el grupo creó es una mezcla de compuestos naturales con células neurales que alimenta a una impresora 3D. Este modelo había sido desarrollado en el marco de trabajos anteriores y permite que las células sobrevivan al proceso de bioimpresión, migren en el espacio e interactúen entre ellas como si estuvieran en el tejido nervioso. Según los investigadores, este protocolo se desarrolló con células de ratones, pero emplea materiales biocompatibles que podrán adaptarse a células humanas en el futuro (lea más en: agencia.fapesp.br/37851/).
“Ahora, aparte de los astrocitos, le agregamos neuronas al modelo. Pero como son más sensibles, estas células se agregaron posteriormente: es como si se las sembrase sobre el material bioimpreso. De este modo, las neuronas no solamente se integraron al modelo, sino que también interactuaron con los astrocitos”, explica Bruna Alice Gomes de Melo, primera autora del trabajo, realizado durante su posdoctorado en la EPM-Unifesp.
Los investigadores explican que en el futuro podrán añadirse más tipos de células neurales, lo que incrementará la complejidad del modelo y lo hará acercarse más al tejido neural.
En la actualidad, los otros modelos en tres dimensiones son los organoides y los esferoides, agregados de células que se autoorganizan en cultivos realizados en laboratorio. “Nuestro modelo posee una mayor reproducibilidad que los organoides y los esferoides. Asimismo, puede erigírselo a una escala mayor”, informa Porcionatto.
Un virus adaptado
Los esferoides son estructuras formadas con base en células madre neurales y también se los conoce con el nombre de neuroesferas; y fueron fundamentales para el desarrollo del SARS-CoV-2 adaptado a ratones. Para ello se los incubó durante siete días junto a partículas del SARS-CoV-2 que infecta a los humanos.
Las pocas partículas virales que sobrevivieron y se replicaron fueron entonces aisladas y puestas en un nuevo cultivo de neuroesferas. Este proceso se repitió cuatro veces, y así se obtuvo una cantidad de virus suficiente como para realizar los ensayos.
La secuenciación genética del virus resultante mostró que este perdió mutaciones cuando se lo comparó con el empleado durante la primera etapa de incubación. El coronavirus adaptado reveló también que estaba más cerca de la cepa original de Wuhan que dio inicio a la pandemia.
Linajes de células Vero, normalmente empleados como modelo de infección de humanos, fueron sometidos tanto a la acción del virus normal como a la del adaptado, lo que mostró una baja capacidad de este último para infectar a otras células que no fuesen de ratones.
Un resultado interesante obtenido en el modelo 3D bioimpreso indicó que el virus adaptado posee una capacidad de replicación 30 veces mayor en los astrocitos que en las neuronas, lo que muestra la relevancia de esas células en la infección del sistema nervioso central provocada por el SARS-CoV-2.
“El patógeno podría sencillamente estar presente en las células, pero no replicarse a punto tal de erigirse en un problema para el organismo. Este resultado muestra que existen partículas víricas reproduciéndose y catapultándose fuera de las células, con lo cual pueden infectar a otras”, informa Gomes de Melo.
Asimismo, durante la infección, los investigadores observaron un aumento de la expresión de quimioquinas, moléculas que atraen a las células del sistema inmunitario. Merced a la presencia de estas, se registró una disminución de las denominadas citoquinas inflamatorias.
“Esto significa que nuestro modelo reproduce lo que sucedería en el organismo, por lo cual constituye una mejor opción con respecto a las células en placas bidimensionales, los organoides y los esferoides. Asimismo, en la biotinta que desarrollamos se pueden agregar otras células que parecen estar implicadas en la infección provocada por el SARS-CoV-2 en el cerebro, tales como las microglías y las células endoteliales existentes en la barrera hematoencefálica, que recubre el interior de los vasos sanguíneos del cerebro”, afirma Porcionatto.
Con este modelo, los investigadores esperan no solamente abaratar los costos de las investigaciones de este tipo, sino también disminuir el empleo de animales en laboratorio.
Este trabajo contó también con el apoyo de la FAPESP en el marco de otros tres proyectos (18/12605-8, 19/01255-9 y 21/03684-4).
Puede leerse el artículo intitulado 3D Bioprinted Neural-Like Tissue as a Platform to Study Neurotropism of Mouse-Adapted SARS-CoV-2 en el siguiente enlace: onlinelibrary.wiley.com/doi/10.1002/adbi.202200002.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





