

Imagen: difusión/Blastocell
Científicos de una startup que cuenta con el apoyo de la FAPESP desarrollan un material que mimetiza las condiciones uterinas y que puede redundar en un aumento de un 32 % en la producción embrionaria bovina
Científicos de una startup que cuenta con el apoyo de la FAPESP desarrollan un material que mimetiza las condiciones uterinas y que puede redundar en un aumento de un 32 % en la producción embrionaria bovina
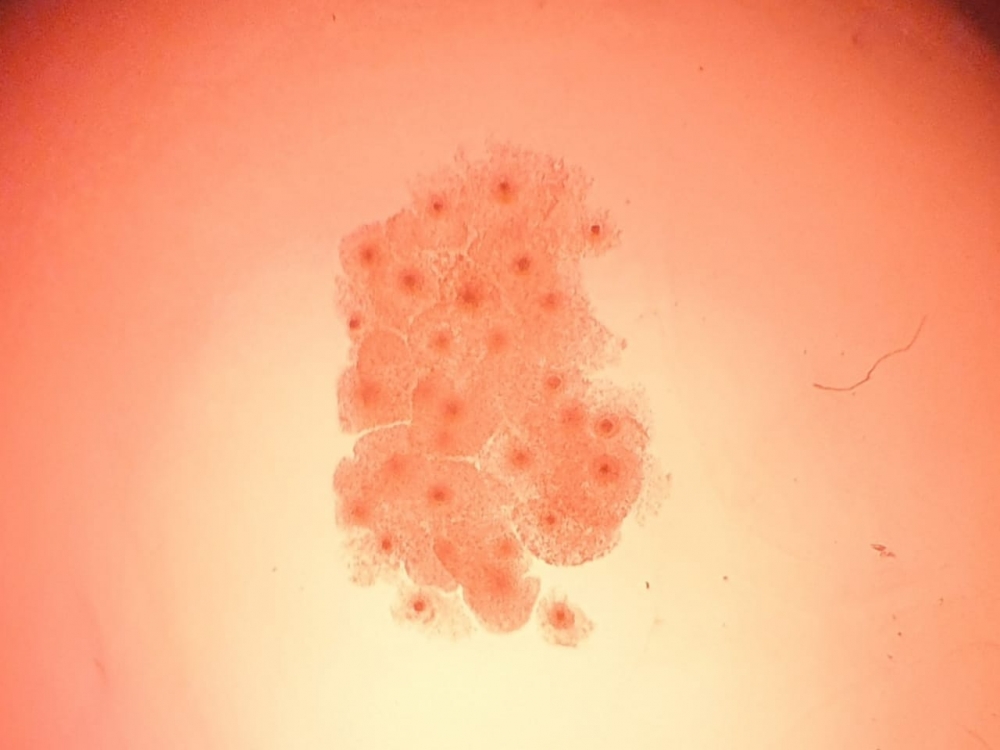
Imagen: difusión/Blastocell
Por Roseli Andrion | Agência FAPESP – A la veterinaria Raquel Zaneti Puelker, cofundadora de la startup Blastocell Biotechnologies, con sede en la localidad de Presidente Prudente, en el estado de São Paulo, Brasil, y especialista en la producción in vitro de embriones bovinos, la asaltaba un cuestionamiento bastante recurrente. La investigadora se preguntaba por qué el cultivo embrionario se concreta actualmente en placas achatadas de dos dimensiones en vez de hacérselo en ambientes en tres dimensiones, tal como se plasma en el interior del útero de esos animales.
“En el actual proceso de producción in vitro es común que el embrión en la gota de cultivo quede pegado en el fondo de esas placas achatadas bidimensionales. A la hora de despegarlo, en lugar de ser una esfera, a veces queda también achatado. Por eso empecé a preguntarme si esa área del embrión que queda pegada en el fondo de la placa y que, por ende, no está en contacto con el ambiente, puede perder la capacidad de interacción”, dice Zaneti Puelker.
Esta inquietud la llevó a la investigadora a pensar en un ambiente más propicio para el desarrollo de embriones in vitro. “Si pudiésemos concretar el cultivo de la manera más cercana a la que transcurre dentro del animal, no se produciría el achatamiento del embrión como sucede en las placas. Al fin y al cabo, tanto en el oviducto [que hace posible el paso de los óvulos desde los ovarios hacia el útero] como en el propio útero, éste permanece en ambientes tridimensionales y en interacción con los tejidos”, explica.
Con base en esta constatación, la investigadora y sus colaboradores Sarah Nunes y Anthony Castilho empezaron a buscar una superficie que se adaptase mejor al proceso y se acercase más al modelo fisiológico. “Llegamos a una membrana de material atóxico que, en teoría, se encuadraría muy bien en esta idea del cultivo tridimensional”, afirma Zaneti Puelker. “Probamos los materiales y seleccionamos a aquellos en los cuales el ovocito [el óvulo] y el embrión se adaptan mejor”, añade.
En pruebas preliminares de laboratorio, esta tecnología mostró buenos resultados de maduración en comparación con el cultivo convencional en dos dimensiones. “Logramos un mínimo de un 10 % de expansión en los embriones producidos”, informa Zaneti Puelker. “Buscamos la calidad del embrión, y por supuesto que esto se traduce en más gestaciones”, sostiene.
Según la investigadora, aparte de ser biodegradable, este material está elaborado con una materia prima ampliamente disponible. El sistema puede implementarse fácilmente en las rutinas comerciales de los laboratorios de embriones bovinos y generar un incremento de un 32 % en la producción embrionaria in vitro. “El impacto más positivo se verificó en las razas taurinas, con un aumento en las interacciones celulares y sin efectos negativos en la calidad ovocitaria”, subraya.
Otra ventaja de este sistema, también de acuerdo con Zaneti Puelker, reside en la posibilidad de liberación lenta de cualquier factor: una proteína o un antioxidante, por ejemplo. “Durante el desarrollo embrionario, existen demandas específicas y este material permite efectuar la liberación lenta de elementos interesantes para el embrión”. Esto resulta útil con relación al ambiente de cultivo, por ejemplo. “Debemos promover el mejor medio en cada etapa con el material que representará al ambiente 3D.”
In vitro e in vivo
Según Zaneti Puelker, los embriones desarrollados in vivo poseen una mejor calidad que los que se cultivan in vitro. “Esto puede obedecer a diversas razones, y una de ellas es quizá el modelo de cultivo. El gran objetivo consiste en que el embrión obtenido in vitro sea lo más cercano posible al producido in vivo”, subraya.
En general, los embriones in vivo poseen más células viables, independientemente de la especie animal. “Hemos evolucionado mucho, pero aún existen deficiencias en la conversión de los embriones obtenidos in vitro en las gestaciones. Estimamos que los pequeños avances nos acercarán a lo que sucede fisiológicamente”, sostiene.
Los embriones producidos in vitro gozan de una gran sensibilidad a los procesos de criopreservación –la preservación por medio de la congelación–, cosa que no sucede con los que se cultivan in vivo. En tanto, la tasa de gestación es mayor entre los embriones desarrollados in vivo. Por eso el objetivo de la técnica desarrollada por la startup es que los embriones obtenidos in vitro se vuelvan más viables, a los efectos de que alcancen los mismos índices de gestación que los que se producen in vivo.
La investigadora explica que cualquier incremento del porcentaje de preñez puede representar un aumento considerable de la producción. “Si un criador cuenta con 100 receptoras preparadas para recibir los embriones, ha invertido en esos animales y espera obtener la mayor cantidad posible de gestaciones”, explica.
Idealmente, el laboratorio envía una cantidad de embriones aptos para llegar al menos a las receptoras disponibles. Asimismo, esos embriones deben producir el porcentaje máximo de preñez posible.
Pero esto no siempre se concreta: en general, la tasa promedio excelente de gestaciones con embriones in vitro es de alrededor del 60 % –aunque en la práctica varía del 30 % al 60 %–, mientras que con los embriones in vivo el índice puede llegar al 80 % de preñez. “De elevarlo un 10 % o un 20 %, por ejemplo, esto se traduce en rentabilidad para el criador.”
Como se trata de un proceso en cadena, se concreta también un ahorro en la preparación de los animales. “En nuestra propiedad, por ejemplo, intentamos mantener una cría sostenible. Si tenemos que sincronizar a los animales y posteriormente sincronizarlos de nuevo, produciremos más residuos y desperdiciaremos material”, describe la investigadora. “Intentamos pensar en toda la cadena de producción. Por eso, cuanto más alta sea la calidad de los embriones, menor será el desperdicio.”
Un modelo en cada etapa
Como el proceso de producción de embriones in vitro se compone de distintas fases, el equipo de la startup tuvo que adaptar la técnica a cada una de ellas. El proyecto cuenta con el apoyo del Programa de Investigación Innovadora en Pequeñas Empresas (PIPE) de la FAPESP. El primer paso consistió en diseñar la metodología de la etapa inicial, de la maduración del ovocito. “No hay producción de embriones de calidad sin ovocitos de calidad.”
Actualmente, Blastocell logra implantar el sistema de maduración con un material producido mediante biodigestores. Y ahora debe poner a prueba las etapas de fertilización y de cultivo embrionario. El tiempo de duración de esta última fase varía de acuerdo con la especie animal: mientras que en animales bovinos la transferencia de los embriones se concreta al sexto o séptimo día, en los equinos se realiza entre el octavo y el noveno día.
El material que se emplea para albergar a los embriones es biodegradable y debe mantenerse de modo adecuado durante toda la fase de desarrollo en que se encuentra (maduración, fertilización o cultivo). Los investigadores pretenden desarrollar un sistema que pueda utilizarse con distintos animales, por eso el material debe tener un comportamiento acorde cuando se lo emplea con embriones de distintas especies. Asimismo, pretenden también desarrollar el ciclo completo de cultivo. Para ello serán necesarios otros dos años de investigaciones.
“Es lo que espero, ya que, tras definir la primera etapa, sabemos manipular el material. Al principio tuvimos dificultades, pero hemos avanzado mucho. Creo que los mayores obstáculos han sido superados y ahora es necesaria la adaptación a las distintas etapas de la producción embrionaria.”
La empresa tiene en sus planes emplear la técnica en la producción de embriones equinos, ovinos y porcinos. “Aparte de la producción de carne, el segmento porcino invierte actualmente en minipigs o minicerdos, que se utilizan en la investigación y el desarrollo de tejidos para trasplantes humanos”, recuerda Zaneti Puelker. “Los embriones porcinos producidos de una mejor manera, en un sistema que promueva una mejor calidad de las células, permitirá obtener animales más adecuados.”
De acuerdo con la investigadora, la técnica con la placa de dos dimensiones se utiliza en todo el mundo, y si bien existen otros estudios en curso en el segmento, los métodos son distintos al que están proponiendo. “Existen modelos que se valen de la tecnología microfluídica para evitar que el embrión quede parado en la superficie. No encontré ninguno que se valga de un material maleable en busca de lograr una cercanía con el útero”, afirma.
El nombre de la empresa constituye una mezcla las palabras blastocisto, la designación de uno de los estadios de desarrollo del embrión, y cell, que hace alusión a la calidad de las células del mismo. “Al fin y al cabo, eso es lo que buscamos: la calidad de las células del embrión.”
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





